4大新型治疗方案 特异性杀死淋巴癌
医句话:
对复发或难治性DLBCL患者而言,目前的标准治疗是在救援性化疗后进行自体造血干细胞移植。然而,长者和共病患者可能不适合这种治疗模式。即便接受了完整的治疗,也仅约30%至40%者病情稳定,维持3年无恶化。值得庆幸的是,医学界出现了许多新型疗法,有些也可联合使用以产生增效作用,有助于改善这类患者的预后。
“淋巴瘤(lymphoma)是源于淋巴细胞(一种白血球)恶性转化的一种癌症。根据世界卫生组织最新的血液肿瘤分类,淋巴癌大致可分为两大类:霍奇金淋巴癌(Hodgkin's lymphoma)和非霍奇金淋巴癌(Non-Hodgkin's Lymphoma,NHL)。
NHL是世界上第10种最常见的癌症类型,占2012年癌症确诊病例的2.7%(约39万名患者),同时也是先进国家第7种最常见的癌症类型。国际癌症研究机构(IARC)的数据显示,NHL在2012年是大马第9常见的癌症。
弥漫B大细胞淋巴癌(Diffuse Large B Cell Lymphoma,DLBCL)是一种具有侵略性的NHL,约占大马所有确诊NHL病例之40%至50%。患者常见的症状为淋巴结肿大、无故消瘦、发热和夜间盗汗等症状。这种疾病偶尔会影响淋巴结以外的其他器官,称为淋巴结外疾病。该病的进展十分迅速并具有侵略性,需要立即治疗。
结合疗法治愈率达60%
针对早期确诊的DLBCL,目前的初步治疗采用免疫疗法(单克隆抗体)结合化疗的方式。化疗应用于治疗DLBCL已超过40年,而免疫治疗则是在2006年才获得美国食品及药物管理局(FDA)的批准。相比起单独应用化疗,免疫疗法结合化疗的方式有效地提高了疗效,估计能治愈约50%至60%的患者。
不幸的是,大约30%至40%的患者的病情在对治疗产生初步反应后复发,或是无法在治疗中达到缓解状态,意即难治性疾病(refractory disease)。这类复发或难治性DLBCL的患者的预后一般较差,若不进行治疗,中位生存期估计只有约3至4个月;至于对目前救援性(salvage)治疗方案无反应的患者,中位生存期只有5至7个月。
救援性化疗加干细胞移植
对复发或难治性患者而言,目前的标准治疗是在采用与初步治疗不同的救援性化疗后,进行自体造血干细胞移植(ASCT)。然而,长者和患有其他疾病的患者可能不适合这种治疗模式。在可接受此治疗方案的患者中,大约50%对救援性化疗产生反应,而产生反应的患者之中,只有50%能够进行自体造血干细胞移植。
对救援性化疗产生反应并接受移植的患者中,仅约30%至40%的病情稳定,维持3年无恶化。事实上,根据美国126家血液学或肿瘤学机构对2010至2016年的真实世界数据分析,在接受救援性化疗并打算接受自体造血干细胞移植的患者中,只有13%实际上进行了移植。
很显然的,目前的治疗方案尚未能满足体弱和年长患者,甚至是年轻或健壮的复发或难治性DLBCL患者的需求。
某些疗法已准使用
值得庆幸的是,医疗界在了解DLBCL生物学方面已取得了重大进展,因此目前或在不久的将来会有大量的新型疗法可提供复发或难治性疾病患者。这些新的治疗策略有望改变治疗此病患者的模式,以满足先前所提的需求。
在这些新的治疗模式中,某些疗法已获批准使用,有些则可能在不久后获批,包括新型和增强型的单克隆抗体、抗体-药物复合体(Antibody-Drug Conjugates,ADCs)、免疫调节剂、双特异性T细胞衔接抗体(BiTEs)、分子通路抑制剂或小分子抑制剂、表观遗传修饰药物(epigenetic-modifying drug)、免疫检查点抑制剂,以及新型细胞疗法,如嵌合抗原受体T细胞(Chimeric Antigen Receptor T cells,CAR-T)以及嵌合抗原受体自然杀手细胞(Chimeric Antigen Receptor Natural Killer Cells,CAR-NK)。
(一)ADCs
现在我们拥有针对DLBCL癌细胞的新型和增强型单克隆抗体。与化疗分子或其他细胞毒性(即‘杀死细胞’)分子结合的单克隆抗体,称之为ADCs,带来了巨大的希望,部分也已获批用于治疗复发性或难治性DLBCL。
传统的单克隆抗体并无化疗部分,而传统的化疗也有脱靶副作用。通过静脉注射给药的ADCs的不同之处在于以淋巴癌细胞为目标,选择性地将化疗剂运输到癌细胞中。相比起传统的救援性化疗,ADCs在杀死淋巴癌细胞上具有更好的特异性。
(二)双特异性抗体
双特异性T细胞衔接抗体(BiTEs)是经过改造的抗体,通过静脉输液给药。BiTEs拥有两个抗原结合臂(arm),一个能识别淋巴瘤细胞表面的分子,另一个可识别T细胞表面的分子。因此,BiTEs能够让T细胞可结合到DLBCL上,从而杀死癌细胞。我们可以说这些药物是利用患者自身的免疫系统来选择性消除淋巴癌细胞。
(三)小分子抑制剂
最新的淋巴癌生物学方面突破强调了淋巴癌细胞和周围的正常细胞(称为‘微环境’)以及免疫系统之间的相互作用对促进淋巴癌细胞存活和增生的影响。某些药物,一般称之为免疫调节剂,可以改变微环境和免疫系统,从而增加癌细胞的死亡。
小分子抑制剂则是针对淋巴癌细胞中某些固有的‘信号通路’,令癌细胞程序性死亡(programmed cell death,触发原先预存在细胞内的死亡程式,进而导致细胞主动性死亡的方式)。
与传统化疗不同的是,小分子抑制剂对正常细胞的影响往往会较小,并且可以更有选择性地消除淋巴癌细胞。大多数的小分子抑制剂可以口服。
(四)嵌合抗原受体T细胞(CAR-T)
在CAR-T疗法中,取自患者血液的T细胞会在实验室中添加人造受体,称之为嵌合抗原受体(CARs),这有助于T细胞识别、瞄准并杀死癌细胞。改造后的CAR-T细胞将会输注回患者体内。与BiTEs不同的是,CAR-T疗法涉及了利用病毒载体对患者自身的T细胞进行基因改造,使T细胞能够表现嵌合抗原受体。

马大医药中心临床血液内科顾问
方案可联用 或可弃化疗
先前所提的治疗模式可以联合使用,以产生增效作用;某些治疗组合甚至可以不使用化疗。实际上,当DLBCL复发或对标准化疗持有抗药性时,这对患者、照护者以及家庭成员甚至是医生而言都是很痛苦的。举例,我曾遇见一名患有DLBCL的长者在经过初步的标准免疫疗法(单克隆抗体)和化疗后达到了缓解,但在几年后又复发了。他接着接受了标准的救援性化疗和自体造血干细胞移植。
不幸的是,在不到1年的时间病情再度复发。一般来说,这意味着预后会较差,而且基于年龄的因素,他并不适合进行更为激进的化疗。后来,他接受了结合免疫疗法(单克隆抗体)和免疫调节剂的治疗方法,并维持良好反应,意即完全缓解。
因此,随着淋巴癌治疗方法的最新突破性进展,复发或难治性DLBCL的预后将获得改善,这一点确实让人感到乐观。及早治疗复发疾病,以及患者,医生和家属或照护者之间的团队努力与合作,也是确保治疗成效的关键。”
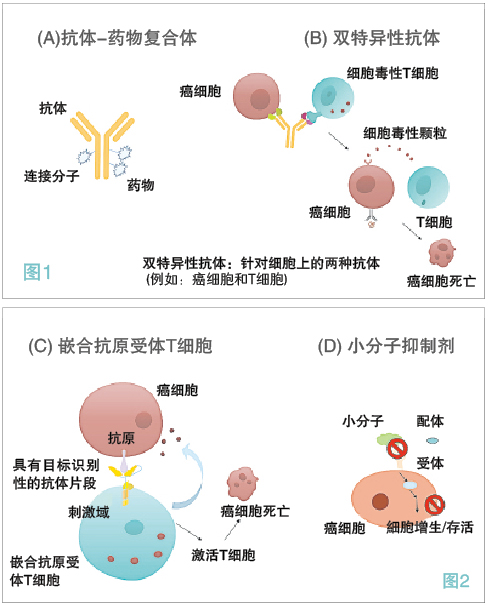
不同疗法在体内的作用机制
A:ADCs确保抗癌药物通过抗体运输到体内的特定部位。
B:双特异性抗体可以靶向两个不同细胞,支持免疫系统杀死癌细胞 。
C:CAR-T细胞是通过改造特定的人类血细胞(T细胞)以识别和杀死癌细胞。
D:小分子抑制剂阻断了癌细胞和体内其他信号互动的方式,使癌细胞生长受到限制。
淋巴癌3问:新疗法适用于復发难治性病例
问1:哪些是淋巴癌的风险因素?
答:大多数淋巴瘤病例中都找不出确切“成因”。淋巴癌本身有许多风险因素,像是曾感染某些病毒如爱泼斯坦-巴尔病毒(Epstein-Barr Virus,EBV)、免疫受抑制如爱滋病患、服用免疫抑制剂的器官移植者,或曾曝露于致癌的化学或辐射等。
问2:DLBCL是如何分期的?
答:通常会使用正子电脑断层扫描(PET/CT),再加上骨髓环钻活检(trephine biopsy)。我国大多数的DLBCL病例往往在更晚期的阶段才被诊断出来。需要注意的是,患者的存活率预测是基于多种因素的,并不只是基于早期或晚期。临床已有许多包含不同参数的分级系统。
问3:哪些前述疗法已被我国批准使用?
答:一些ADCs、BiTE和小分子药剂已获批。大马数间私人医疗中心也提供CAR-T疗法。这些药物本身不适用于早期DLBCL,主要用于DLBCL的复发和难治性病例(无论分期为何)。它们用于那些不能接受自体造血干细胞移植的患者。然而,它们在许多情况下也被用作“救援性”疗法,以便达到缓解,并让患者可接受移植。
温馨提醒:文章与广告内提及产品、服务及个案仅供参考,不能作为看诊依据,须以医生的意见为主。













评论