新长效胰岛素.减轻药担疗效佳
甘精胰岛素(insulin glargine),适用于一型及二形糖尿病患。
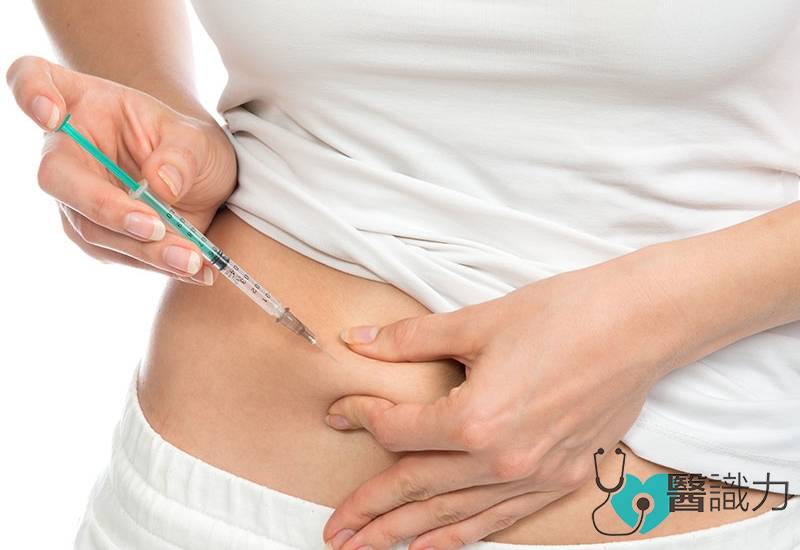
它可取代其他无法24小时发挥药效的胰岛素,患者在注射一次后可获得较长时间疗效,也达致降低血糖的效果。
我国引进首个甘精胰岛素(insulin glargine)生物相似药Basalog,与原研药相比,此药物无论在安全性、耐受性及疗效层面皆被证实取得相同生物等值(bioequivalent),患者在可负担价格下使用高素质的药物,无疑是一项好消息!
当患者在皮下注射新药溶液,其酸性溶液被中和后,所形成的微细沉积物可持续释放少量甘精胰岛素,继而产生长达24小时平稳无峰值的血药浓度。
新药的结构及生产技术复杂,透过基因工程处理过的活细胞培养生产后,再发酵、纯化、结晶化、调制药物配方等步骤而成。
生物相似药是当原厂生物制剂(即大分子药物)在专利保护到期之后,其他药厂利用现有的数据进行仿制及生产的药品。
欧盟、美国、印度及日本普遍上对生物相似药的定义,设为与原研药在品质、生物活性、安全性及有效性都能达到相似的认定。
这些国家订制明确的审查程序及规范,药厂依循法则要求生产生物相似药,并进行药物代谢动力学(PK)及药效动力学(PD)试验,以证明其安全与疗效。
日本已核准上市
日本是一个对生物相似药物高度监管的国家,而新药获得日本的批准,无疑对此药建立一个值得信赖的里程碑。
日本的PK及PD试验显示,新药与原研药的主要及次要研究终点皆取得相等成果。
日本就新药与原研药进行临床第三期研究,共有260名接受深切治疗的一型糖尿病的患者参与为期52周的研究。
研究显示,分别服用新药及原研药患者的糖化血色素(HbA1c)及饭前空腹血糖(FPG)水平相似,且胰岛素剂量及糖尿病治疗满意度问卷(DTSQ)评估无差异。另外,两组病患的血糖过低症及药物不良状况相似,抗甘精胰岛素抗体及抗胰岛素抗体的阳性反应也没有差别。

拉玛亚医药学院及医院教授(印度)

内分泌内科顾问(吉隆坡)
总结:减低药物开支
新药与原研药为一型糖尿病患者皆提供相似的血糖控制及安全性效果。
目前,针对一型及二型糖尿病患者使用新药,而展开的国际第三期临床试验仍在进行中。
全球糖尿病的医疗费用高涨,患者的药物费用也相对增加,然而生物相似药的出现发挥减低药物开支的功效。
西太平洋区域于2015年的糖尿病医疗支出高达1亿5320万令吉,预计在2020年,此数据将飙高至2亿1480万令吉。”
高涨的医疗费用导致病患无法获得高品质的医疗服务,而且难以负担药物费用。
生物相似药提供可负担药物的优势,为美国未来10年省下400亿至2500亿美元的费用,让更多发展中国家的人民可负担药费。
市场上目前有450种生物相似药,另有250种药正在研发中,分析师预计到2020年生物相似性药品市场将达到250至350亿美元的规模。
可与原研药交换使用
随着多个原厂生物制剂的胰岛素专利保护到期,患者对胰岛素生物相似物的需求将会提高。
国内近年来越来越多糖尿病患者接受胰岛素治疗,到底这些接受胰岛素治疗的患者,是否达到建议升糖指数标准呢?
胰岛素共分为五大类别,包括短效、中效、快速胰岛素类似物、基础类似物及混合型胰岛素。
胰岛素生物相似药乃“复制”原研药,两者之间的氨基酸序列相似,惟在临床及分子特征上稍微有区别。
基于生物相似药无需负荷研发及全规模临床试验的成本,因此生物相似药的价格往往比原研药来得低,如此一来,极可能降低糖尿病的治疗成本,患者可更容易获得胰岛素治疗。”
“我国执法单位定制条例,任何生物相似药进入本地市场,必须符合第四阶段的市场后监测程序。
生物相似药作为替代药物,无论在安全、疗效或市场调查层面上,都必须与参考的原研药达到一定的相似度,“为证明药物的相似度,生物相似药得完成符合疗效、安全及比较性的研究。”
若生物相似物超过一次或持续被使用为治疗药物,并与原研药交换使用时,不会带来任何额外风险,即可被定义为替换使用(interchangeable)。
胰岛素生物相似药在获得批准时,已提供大量完整的数据,并进行符合条例的市场后监测。





评论