弥漫性大B细胞淋巴瘤复发 抢时间救命! 搭配免疫化疗 ADC助增反应率存活期
“弥漫性大B细胞淋巴瘤(Diffuse Large B-cell Lymphoma,简称DLBCL)是一种有机会治愈的疾病,但并非每个人都能如此幸运。曾碰过一位让我印象深刻的患者,他的淋巴瘤在第一线治疗缓解多年后又再复发。”林口长庚医院血液科施宣任医生表示,“患者过去曾因罹患肺癌切除过肺脏,身体状况难以承受自体干细胞移植,面临治疗选择相当有限的困境,状况一度很不乐观。”
幸运的是,当时针对DLBCL淋巴瘤的突破性新治疗–抗体药物复合体ADC(Antibody-drug Conjugate)刚好核准通过。根据临床试验数据,针对复发的病患,若于治疗时再加上ADC药物,完全反应率是传统化疗的两倍,整体存活期更较传统化疗增加将近3倍!因此当时在讨论后,立刻帮患者将ADC药物加入治疗组合中,后续也顺利地达到完全缓解快1年,目前没有复发迹象,持续门诊追踪。
复发具抗药性 急需新治疗突破
DLBCL是台湾最常见的淋巴瘤。根据国健署癌症登记报告,台湾1年新增超过4000例淋巴癌个案中有9成属于非霍奇金淋巴癌,超过一半是恶性度很高的DLBCL,不仅进展快速,且可能侵犯全身器官,因此治疗要越快越好,尽量避免等待空窗期。
施宣任医生强调,“不像一些小细胞的低恶性度淋巴瘤可以等症状明显再治疗,大细胞病变通常来势汹汹,像DLBCL虽然会因为分期等因素,治疗选择上略有差异,但基本就是完全不能等!”
过去DLBCL标准的第一线治疗为化疗药物再加上CD20单株抗体的免疫化学治疗,除化疗毒杀肿瘤细胞外,同时借由单株抗体直接促使带有CD20的B细胞死亡达到缓解的效果。
“大约5至6成的病患接受免疫化学治疗后可以达成长期完全缓解也就是痊愈;剩下无法完全缓解的这群病患,又被称作顽固型DLBCL淋巴瘤,因为已经对第一线药物产生抗药性,治疗上较为棘手,需要更有效的新药物选择。”


让淋巴瘤细胞“吞下化疗”
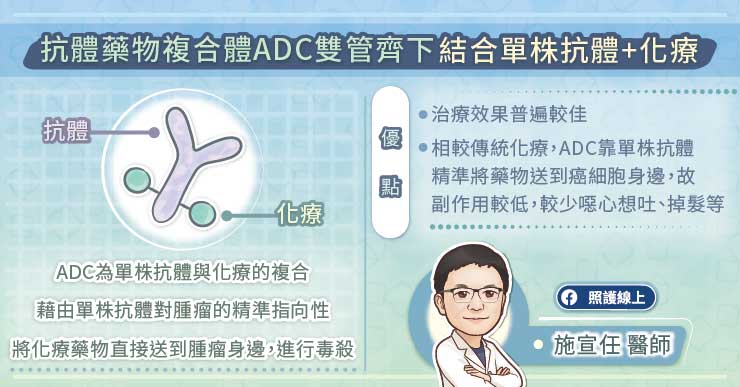
ADC是经临床试验证实有效DLBCL淋巴瘤治疗的新突破选择。ADC药物的“复合”二字,指的就是单株抗体与化疗的结合,借由单株抗体对肿瘤的精准指向性,将化疗药物直接送到肿瘤身边,进行毒杀。
施宣任医生进一步解释,“ADC药物的专一性优势,除了让治疗效果更显着外,相较传统化疗没有目标性地作用,ADC药物透过单株抗体可达成如同让淋巴瘤细胞直接把化疗吞进去的效果,自然副作用也降低很多,病患比较少感觉恶心、想吐、掉发等。”
临床研究显示,ADC药物合并免疫化学治疗一起使用后,能够增加顽固型或复发淋巴瘤病人的整体存活期和完全反应率,并具有更长的疗效持续时间。
存活期延长3倍 反应率也倍增
“整体存活期约增加近3倍、达成完全反应的几率则增加2倍以上,对已产生抗药性的病人来说,这样的数字实属难能可贵。”施宣任医生指出,因此美国NCCN治疗指引也建议,符合特定条件的DLBCL淋巴瘤病人,可优先考虑接受ADC药物的治疗组合。
“台湾的医疗基本都是与国际同步,特别会参考美国的作法,因此健保署也于2024年2月将ADC纳入DLBCL淋巴瘤第三线给付,让患者能够在减轻经济负担的状态下,快速接受与国际同步的最新治疗。”
治疗期间应避开人多场所
现今DLBCL淋巴瘤的治疗已朝多元选择迈进,但免疫化学治疗仍是重要的骨干治疗。施医生提醒,包括ADC药物等不同治疗组合,都会搭配不同的化学药物,毒性虽有高有低,但都可能造成免疫力低下,因此治疗期间,应尽可能降低感染的机会,避免出入人潮较多的公共场所。
“近期流感、COVID-19等呼吸道传染症疾病也较盛行,DLBCL的病人更应提高警觉,小心预防。”
(编按:本文由“照护线上”授权转载。*连接至https://www.careonline.com.tw)

何金华医生(Ho Kim Wah)
血液内科及移植医学顾问
锁定CD79b ADC精准攻克DLBCL
“抗体药物复合体(ADC)虽然已不是全新的药物形式,但近年开始应用在治疗弥漫性大B细胞淋巴瘤(DLBCL)上,带来了新的治疗希望。
要了解ADC的运作,首先我们得认识什么是DLBCL。这是一种来自B细胞的恶性肿瘤,这些肿瘤细胞表面会带有特定的‘抗原’,就像是它们的特征标记。医生可以透过标靶治疗,针对这些抗原来锁定并清除癌细胞。ADC就是一种这样的标靶治疗药物。
在这类药物中,最常见的标靶抗原是CD20,一种存在于B细胞表面的蛋白质。除此之外,还有另一个重要的抗原叫CD79b,也经常出现在B细胞恶性肿瘤中,因此成为研究与治疗的重要目标。
目前用于DLBCL的ADC药物,是将针对CD79b的单株抗体与一种毒杀癌细胞的药物,即MMAE(Monomethyl Auristatin E)结合而成。这种复合药物在注射进体内后,会自动寻找并锁定带有CD79b的B细胞,将化疗药物直接送入癌细胞,进而达到杀死癌细胞的效果。
值得注意的是,ADC通常不会单独使用,而是搭配化疗一同进行,提升治疗效果。
R-CHOP提高存活率至70%
在血癌的治疗中,R-CHOP是目前最常用来对付血液肿瘤,尤其是DLBCL的化学治疗组合。
所谓 R-CHOP,是5种药物的缩写组合,包括Rituximab(利妥昔单抗)、Cyclophosphamide(环磷酰胺)、Hydroxydaunorubicin(即doxorubicin,多柔比星)、Oncovin(学名为vincristine,长春新碱)及Prednisolone(泼尼松龙)。其中泼尼松龙并不是化疗药物,而是一种类固醇,用来抑制发炎反应及杀死部分淋巴细胞。
R-CHOP这个疗法已有多年历史。20世纪末期,随着单株抗体rituximab的加入,治疗效果显着提升,完全反应率从原本的60%提升到76%,整体存活率也从56%增加到70%。
Polatuzumab联用R-CHP 定点杀癌
Polatuzumab vedotin是一种针对B细胞表面抗原CD79b的抗体药物复合体(ADC)。它结合了单株抗体与化疗药物 MMAE,能精准地将药物送入癌细胞中,达到定点杀伤的效果。
在治疗上,polatuzumab通常会与R-CHP(即去掉vincristine的R-CHOP)一起使用。这是因为polatuzumab和 vincristine都可能造成神经毒性副作用,若同时使用,会大幅增加出现周边神经病变的风险,轻则手脚麻木,重则四肢疼痛无力,影响日常生活。
治疗后长时间不复发
此外,polatuzumab本身属于免疫疗法,可能会引起发烧、疲倦、恶心等副作用。但无论是传统的R-CHOP或新的R-CHP+polatuzumab,两者的副作用整体来说差异不大。
不过,polatuzumab 属于较新且复杂的药物,因此治疗费用明显高于传统化疗组合。患者在选择时,必须衡量经济能力与治疗效益。
将polatuzumab加入治疗组合后,病患的无疾病生存率(DFS)与无恶化存活率(PFS)也从70%提升到77%,代表更多患者在治疗后能长时间不复发。
大马一线治疗并用ADC
目前,大马也已开始在一线治疗中使用ADC类药物,为DLBCL病患带来更多治疗选择。
此外,二特异性抗体(bispecific antibody)是一种能同时结合两种不同抗原(或表位)的抗体。它的原理可以形象地理解为‘一对二’,就像一只抗体长了两只手,一手抓住T细胞(即我们的免疫杀手细胞),另一手则抓住肿瘤细胞(例如表面带有CD20的B细胞)。
T细胞识癌展攻击
当这两者被‘拉近’后,T细胞便能直接辨识并攻击癌细胞。这类疗法已被应用于血癌的治疗,并展现出良好的潜力。
造血干细胞移植与嵌合抗原受体T细胞疗法(Chimeric Antigen Receptor T-cell therapy,CAR-T)也是治疗淋巴癌和血癌的重要选项之一。”
**温馨提醒:文章与广告内提及产品、服务及个案仅供参考,不能作为看诊依据,须以医生的意见为主。











评论